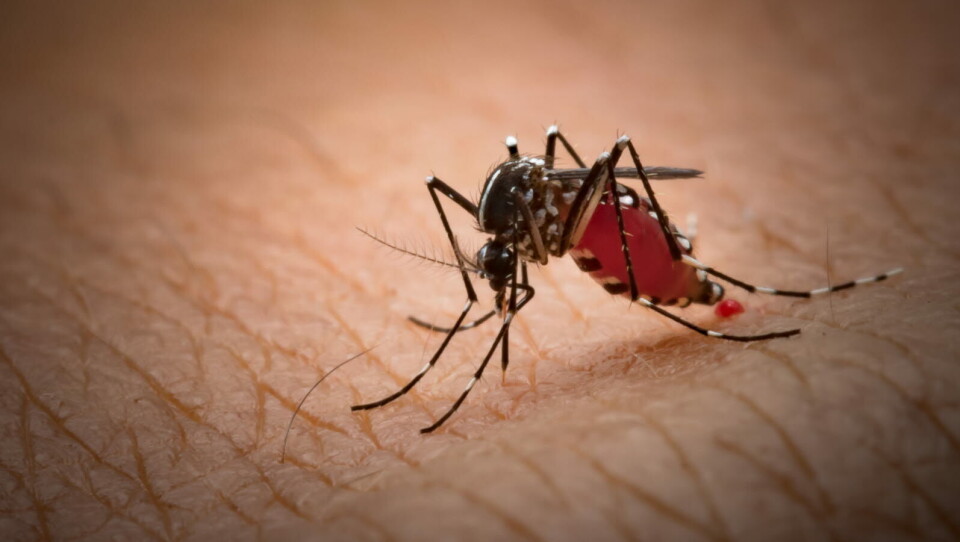
ETT STEG NÆRMERE: Bildet viser en mygg i aedes-familien, som er ansvarlige for spredning av både zikavirus, denguevirus og chikungunya-virus. En vaksine mot sistnevnte virus kan nå nærme seg godkjenning. Illustrasjon: Getty Images
Foto:Gode nyheter for CEPI-støttet chikungunya-vaksine
Det franske vaksineselskapet Valneva møtte primærendepunktet i den aller første fase 3-studien for en chikungunya-vaksinekandidat. De er dermed et steg nærmere å få godkjent verdens første vaksine mot den smittsomme sykdommen.
Denne artikkelen er mer enn tre år gammel.

Topplinjeresultatene fra den avgjørende fase 3-studien med selskapets enkeltdose vaksinekandidat mot chikungunya, VLA1553, viser at vaksinen induserte beskyttende nøytraliserende antistoffer mot sykdommen i 98,5 prosent av studiedeltakerne. Dette ble oppnådd 28 dager etter enkeltdosen.
Studien inkluderte 4115 voksne over 18 år, og ble gjennomført på tvers av 44 studiesteder i USA. Vaksinen var godt tolerert av studiedeltakerne.
Ifølge Valneva overskredet beskyttelsesraten amerikanske legemiddelmyndigheters (FDA) krav for godkjenning på minst 70 prosent beskyttelse. VLA1553 fikk nylig også såkalt Breakthrough-status av FDA, som gir muligheter for raskere godkjenning av vaksinen.
Har fått millioner i støtte fra CEPI
I 2019 signerte selskapet en partneravtale med Coalition for Epidemic Preperadness Innovations (CEPI). CEPI har støttet selskapet med opp til 23,4 millioner dollar, som skulle gå til produksjon av og senfase-studier på vaksinekandidaten.
Frederik Kristensen, nestleder i CEPI, skriver i en e-post til Dagens Medisin at dette er de første fase 3-resultatene for en vaksine mot chikungunya noensinne.
– Resultatene viser at vaksinen er svært effektiv og trygg, og er et stort skritt forover på veien mot en tilgjengelig vaksine mot denne alvorlige sykdommen. Chikungunya medfører store lidelser og økonomiske tap. CEPIs finansiering muliggjør tilgang til vaksinen for mennesker i lav- og mellominntektsland hvor sykdommen ofte er endemisk. Avhengig av regulatorisk godkjenning, vil denne vaksinen vil bli et viktig redskap for å beskytte sårbare grupper mot en stor folkehelse-risiko.
– Positive resultater av våre investeringer
Han påpeker at etableringen av CEPI i 2017 nettopp ble gjort for å utvikle vaksiner mot sykdommer som kan utvikle seg til epidemier eller pandemier.
– Det er veldig gledelig at vi nå ser konkrete og positive resultater av våre investeringer. Å utvikle vaksiner mot sykdommer som chikungunya er en viktig del av et globalt forsvar som i framtiden kan gjøre oss i stand til å stanse utbrudd av smittsomme sykdommer før de rekker å utvikle seg til epidemier eller pandemier.
Kan få alvorlige følger
Chikungynuyavirus-sykdom, eller chikungunuyafeber, er ifølge Folkehelseinstituttet (FHI) en virussykdom som overføres med enkelte mygg fra slekten Aedes. Sykdommer forekommer ifølge FHI normalt i Afrika, Asia og det amerikanske kontinent.
De fleste som smittes får ikke symptomer, men de som får symptomer opplever ofte feber, hodepine og ledd- og muskelsmerter. Hos normalt friske personer går sykdommen over av seg selv, men gravide og personer med nedsatt immunforsvar og andre kroniske sykdommer kan få mer alvorlig sykdom som lunge- og hjertesvikt og infeksjon i sentralnervesystemet.
– Vi er svært glade for at disse fase 3-resultatene bekrefter den overbevisende profilen til vår vaksinekandidat på tvers av alle aldersgrupper. Disse første fase 3-studieresultatene for en chikungunya-vaksine noensienne betyr at vi er et steg nærmere å kunne adressere denne store, voksende og umøtte folkehelsetrusselen. Jeg vil takke alle som har deltatt i studien, og som fortsetter å ta studien videre under pandemien. Vi vil fortsette å jobbe med regulatoriske myndigheter for å bringe VLA1553 til marrkedet så raskt som mulig, sier Juan Carlos Jaramillo, medisinsk direktør i Valneva, i en uttalelse fra selskapet.
















